Die modernen Biowissenschaften entwickeln sich so schnell, dass die ethische Bewertung nicht mehr mitkommt. Transgene Pflanzen, Impfstoffe, personalisierte Medizin, riesige Datenbanken mit sehr persönlichen Informationen – brauchen wir das alles oder sollten wir zunächst innehalten und zuerst sorgfältig alle möglichen Konsequenzen untersuchen? Die Frage geht weit über die philosophischen Aspekte hinaus und sollte praktische Überlegungen zu Gesundheit, Ernährung und Nachhaltigkeit einschließen, aber auch die Auswirkungen auf Innovationspotenzial, Wirtschaft und Wettbewerb. Der folgende Artikel stammt aus der Feder eines „Couch-Philosophen“, der mehr Fragen als Antworten in der ethischen Debatte sieht. Ich möchte damit anregen, die ethischen Betrachtungen auch im Kontext mit der Praxis und den Konsequenzen für unsere Gesellschaft zu diskutieren und freue mich auf sachliche Kommentare.
Warum sind genetische Daten gleichzeitig wichtig und ethisch brisant?
Dieser Artikel beruht auf einer Publikumsfrage bei der ICOBIOS in Malang, Indonesien am 25.10.2025, wo ich einen der Hauptvorträge über „Gene, Genome und Metagenome“ halten durfte. Eine Teilnehmerin fragte anschließend: „Welche ethischen Probleme sehen Sie in der umfassenden Erhebung persönlicher genetischer Daten?“
Die Frage ist mehr als berechtigt. Was man aus genetischen Daten inzwischen (mehr oder weniger zuverlässig) ableiten kann, ist gewaltig. DNA- und RNA-Analysen erlauben immer genauere Aussagen über genetisch bedingte Krankheitsrisiken und aktuelle Infektionserkrankungen. In einem früheren Blogartikel hatten wir schon über erste Versuche berichtet, aus einer DNA-Spur an einem Tatort ein „Täterfoto“ abzuleiten (https://www.biowisskomm.de/2022/11/phantombilder-aus-dna-analyse/). Aus Luftfiltraten kann man anhand von DNA-Sequenzierung feststellen, wer sich in einem Raum aufgehalten hat https://www.scinexx.de/news/biowissen/erster-nachweis-von-dna-aus-der-luft/. Angeblich achten hochrangige Politiker akribisch darauf, bei Konferenzen keine DNA Spuren zu hinterlassen. Sie könnten Hinweise auf persönliche Eigenschaften oder Krankheiten liefern oder sogar „personalisierte“ Attentate erlauben. Ob Politiker ihre Atemluft und ihren Hautabrieb unter Kontrolle bringen können ist eher fraglich.
Kann man die Erfassung und Auswertung solcher Daten z.B. durch staatliche Institutionen, Versicherungen, Arbeitgeber und andere überhaupt noch zuverlässig regulieren?
Andererseits sind diese Daten unverzichtbar, wenn man Krankheiten verstehen und Therapeutika entwickeln will.
Daten-Naivität oder ein Beitrag zur Forschung?
Es ist bemerkenswert, dass ca. 15 Millionen Kunden der Firma 23andMe ihre DNA zur Analyse zugeschickt und dafür sogar Geld bezahlt haben. 80% der Kunden haben der Datenverwertung für die Forschung zugestimmt, andere Nutzungen sind nicht ausgeschlossen. 2023 wurde 23andMe gehackt. Sieben Millionen Datensätze (inklusive persönlicher Angaben) wurden gestohlen und vermutlich im Darknet verkauft.
Eine absolute Datensicherheit kann nie gewährleistet werden. Ob allen Kunden, trotz obligatorischer, umfangreicher Aufklärung, die möglichen Konsequenzen bewusst sind, kann man bezweifeln.

Was tun die kommerziellen Genomsequenzierer?
23andMe sequenzierte keine vollständigen Genome. Stattdessen wurden Microarrays verwendet, auf denen zehntausende bekannter Genvarianten aufgetragen waren, die auf genetisch bedingte Krankheiten, äußerliche Merkmale, Abstammung und mehr hinweisen. Dazu gehören z.B. auch Veranlagungen zu psychischen Erkrankungen. Vereinfacht gesagt, filtert diese Genotypisierung aus dem riesigen menschlichen Genom solche DNA-Sequenzen aus, die nach dem Stand der Forschung eine Relevanz haben. 2021 hatte das Unternehmen einen Börsenwert von 6 Milliarden Dollar. Im März 2025 ging 23and Me insolvent und wurde vom TTAM Research Institute (non-profit Unternehmen) für 305 Millionen Dollar gekauft.
Ein weiteres Unternehmen ist MyHeritage, das auch Analysen über Microarrays, inzwischen aber ebenfalls „Whole Genome Sequencing“ anbietet. Fast makaber finde ich, dass MyHeritage die DNA-Sequenzierung im „Black Friday Sale“ auf Social Media anbietet. Etliche weitere Unternehmen bieten ähnliche Produkte an. Sehr persönliche Daten sind zu einem kommerziellen Produkt wie Socken oder eine Blumenvase geworden.
Im Prinzip ist es bereits jetzt möglich, mit etwas Grundkenntnissen zur Molekularbiologie und Bioinformatik und einer Ausstattung im Wert von 2000€ bis 3000€ eine vollständige DNA-Sequenzierung in jedem „Küchenlabor“ durchzuführen. Eine Kontrolle oder Regulierung wird vermutlich sehr bald kaum noch möglich sein. Besonders bei Daten, die Hinweise auf genetische Erkrankungen liefern, ist es sehr problematisch, die Kunden und Nutzer mit dieser Information alleine zu lassen. In den meisten Fällen werden sie die Daten ohne fachliche Begleitung kaum richtig interpretieren können und möglicherweise zu falschen Schlussfolgerungen kommen, wenn die Veranlagung zu einer erblichen Erkrankung angezeigt wird.
Big Data und Datenschutz
Ein vollständiger Schutz sensibler Daten kann niemals garantiert werden. Die Brisanz individueller genetischer Daten ist offensichtlich. Diverse Möglichkeiten sie zu missbrauchen liegen auf der Hand: Versicherungen könnten genetische Risiken einpreisen, Arbeitgeber könnten Bewerber aufgrund genetischer Veranlagungen ablehnen. Das bringt unzählige ethische Probleme und Fragen mit sich: Wenn jemand seine genetische Prädisposition für eine schwere Krankheit kennt, darf er sie dann einer Versicherung verheimlichen? Darf er eine hohe Lebensversicherung abschließen? Muss ein Pilot oder Busfahrer seinem Arbeitgeber ein ihm bekanntes genetisches Risiko (z.B. psychischen Erkrankung oder Herzinsuffizienz) melden? Darf man von einem Arbeitnehmer einen Gentest verlangen, um Risiken zu minimieren? Sollte man vor der Zeugung eines Kindes eine genetische Analyse empfehlen, um die Ausbreitung genetisch bedingter Krankheiten zu vermeiden? (Dies wird tatsächlich bereits seit Jahrzehnten im weltweit größten Eugenikprogramm praktiziert.)
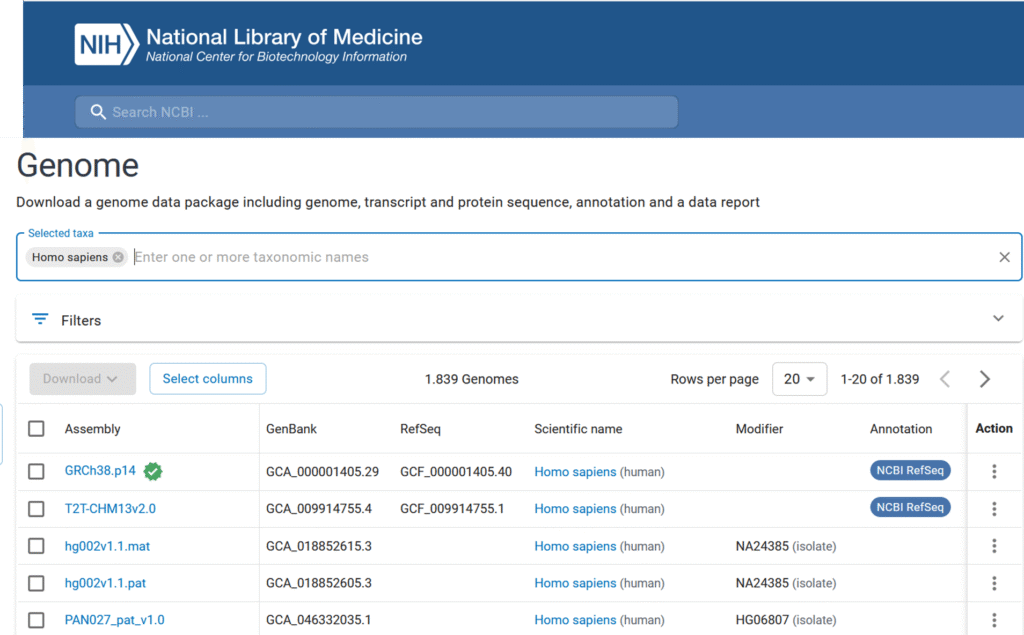
Aber es ist weit mehr als das. Die zunehmende Menge an Daten hat allein bei 23andMe zu mehreren Updates der Datenanalyse geführt. Mehr relevante Genvarianten wurden identifiziert und mehr Gene, die Kandidaten für Krankheiten oder psychische Probleme, Unverträglichkeiten, Resistenzen und äußerliche Merkmale sind. Der Informationsgehalt der Genotypisierung nimmt ständig zu.
Gleichzeitig nimmt sich die Pharmaindustrie diese Daten vor und entwickelt Medikamente und Therapien. Auch sehr seltene Krankheiten können mit Hilfe personalisierter Medizin inzwischen erfolgreich behandelt werden.
Darf man Daten verwenden, die unter ethisch fragwürdigen Bedingungen gesammelt wurden?
In der Wissenschaft galt lange Zeit die Regel, dass Forschungsdaten (ggf. anonymisiert) öffentlich zugänglich sind und international geteilt werden. Dieses System ist löchrig geworden. Durch die umstrittene DSI-Gesetzgebung (digital sequence information) sollen Länder das exklusive Recht auf ihre DNA Sequenz-Daten erhalten – genetische Daten verschwinden so hinter einer Pay Wall und die Länder bestimmen wer und zu welchem Preis darauf Zugang hat (das gilt für Sequenzdaten von Menschen, Tieren, Pflanzen und Mikroorganismen).
Welche Daten von Firmen und in Ländern mit weniger transparenter Wissenschaft gesammelt werden, wissen wir nicht unbedingt.
Durch unterschiedliche Gesetzgebungen wissen wir auch nicht immer, nach welchen ethischen Regeln selbst öffentlich zugängliche Daten und Ergebnisse erhoben wurden. Dürfen wir überhaupt solche Daten mit unklarem oder fragwürdigem Ursprung verwenden?
Ein Beispiel dafür sind die drei „CRISPR-Babys“, die 2018 in China geboren wurden. Das Experiment, bei dem in der Keimbahn der Kinder das CCR5-Gen „abgeschnitten“ wurde, war (für unsere Standards) jenseits aller ethischen Maßstäbe. Folglich weigerten sich mehrere große wissenschaftliche Zeitschriften die Arbeit zu veröffentlichen. Andererseits wird dem Wissenschaftler He Jiankui vorgeworfen, dass er die Versuche nie veröffentlicht hat.
Welche Experimente und medizinische Eingriffe in anderen Ländern und anderen Kulturen legal oder illegal sind, unterscheidet sich schon in der Gesetzgebung: Die Herstellung embryonaler Stammzellen ist in Deutschland verboten, in Israel nicht. Leihmutterschaft ist in vielen Ländern erlaubt, in Deutschland nicht. Die Experimente von He Jiankui wurden vom chinesischen Staat großzügig gefördert, erst später, als es eine weltweite Entrüstung gab, hat man sich offiziell davon distanziert. Gleichzeitig erfolgte eine (inoffizielle) Nachrichtensperre.
Es ist denkbar, dass das Experiment der CRISPR-Babys völlig gescheitert ist, die Kinder schwere Schäden erlitten haben oder bereits gestorben sind. Das würde voraussichtlich dazu führen, dass weitere Experimente (zunächst) eingestellt werden.
Oder das Experiment war, trotz aller technischer Mängel, ein voller Erfolg. Das würde, unabhängig von ethischen Bedenken, wahrscheinlich in einigen Laboren den Ehrgeiz und die „Experimentierlust“ beschleunigen.

Mit an Sicherheit grenzender Wahrscheinlichkeit sind die Genome der drei Kinder inzwischen vollständig sequenziert. Ebenso wird man in China wissen, ob die erwarteten Ergebnisse (verbesserte Neuroregeneration, verbessertes Gedächtnis und HIV-Resistenz) erzielt wurden
Will man, darf man oder muss man diese Ergebnisse kennen?
Viel hilft viel – bei Sequenzdaten kommt es auf Masse an.
Die Datenfülle bringt ethische Risiken, gleichzeitig ist sie eine unabdingbare Voraussetzung für medizinischen Fortschritt.
Die DNA-Sequenzierung ist schon lange keine „Rocket-Science“ mehr. Mit sehr preisgünstigen Geräten (ab 1.000€) und etwas Know-How können Milliarden an DNA-Basen innerhalb weniger Stunden sequenziert werden.
Masse ist wichtig. Je mehr Datenmasse, umso besser die Signifikanz zwischen bestimmten DNA Sequenzen und der „Ausprägung“ einer bestimmten Eigenschaft (wie z.B. einer erblich bedingten Krankheit). Daraus ergeben sich dann Möglichkeiten, Therapien zu entwickeln, die teilweise für seltene Mutationen maßgeschneidert werden können.
Wer viele Daten hat, kommt schneller zum Ziel. Länder mit weniger strengen Regeln können leichter, schneller, billiger, mehr Daten ansammeln. Und sicherlich ist es auch einfacher, unter ethisch fragwürdigen Bedingungen, Therapien „auszuprobieren“. Gerade sogenannte „seltene Erkrankungen“ (weniger als 5/10.000 Menschen, manche sind deutlich seltener) stellen eine große Herausforderung dar, den genetischen Ursprung zu finden.
Eine weitere Herausforderung sind multigene Erkrankungen, d.h. das Zusammenwirken mehrerer Mutationen ist erforderlich, damit sich eine Krankheit manifestiert. Auch hier sind sehr große Datenmengen erforderlich, um solchen Interaktionen auf die Spur zu kommen.
Das ethische Dilemma
Will man beispielsweise bei Gentests persönliche Daten möglichst sicher schützen und die Datenerhebung ethisch einwandfrei durchführen, so macht man Forschung komplizierter und aufwändiger. Gleiches gilt für klinische Studien und auch für Tierversuche. Umfangreiche Genehmigungsverfahren und organisatorische Maßnahmen sind erforderlich. In unserer Gesellschaft ist das weitgehend akzeptiert – in anderen Gesellschaften gelten andere Regeln, andere ethische Standards.
Strenge ethische Regeln schaffen wissenschaftliche Nachteile: man braucht mehr Zeit und mehr Geld und manche Experimente sind gar nicht durchführbar. Das bedeutet nicht, dass man die Regeln über Bord werfen sollte. Wir müssen uns aber dessen bewusst sein und Lösungen finden, um im intellektuellen sowie im wirtschaftlichen Wettbewerb mithalten zu können. Und wir müssen Konflikte in Betracht ziehen, die zweifellos durch unterschiedliche ethische Standards entstehen werden. Wenn z.B. China neue Medikamente und Therapien entwickelt, wird man deren Zulassung in Europa von den ethischen Bedingungen der Datengewinnung und Produktentwicklung abhängig machen? Wird die Entwicklung überhaupt ausreichend transparent dokumentiert, um das beurteilen zu können? Wäre es andererseits ethisch vertretbar, Kranken ein funktionierendes Medikament zu verweigern, weil seine Entwicklung nicht unseren ethischen Standards entsprach?
Hinzu kommt die Schere zwischen arm und reich: darf man medizinische Behandlungen zulassen, wenn nicht jeder gleichermaßen dazu Zugang hat? Wohlhabende werden immer mehr oder weniger legale Wege finden, eine Behandlung in einem anderen Land mit eher lockeren Regeln zu bekommen.
Priorität für ethische Standards?
Nun kann man argumentieren, dass ethische Standards unabhängig von wissenschaftlichem Erfolg oder Misserfolg höchste Priorität haben. Im Falle von Medikamenten, die in anderen Ländern unter ethisch fragwürdigen Bedingungen entwickelt wurden, entsteht dabei jedoch ein neues ethisches Problem: ob Ärzte nach dem Genfer Gelöbnis (moderne Fassung des hippokratischen Eids) handeln, wenn sie einem Patienten eine heilende Therapie verweigern, kann man hinterfragen. Handeln Patienten oder deren Angehörige unethisch, wenn sie ein Medikament fordern, das Heilung bringt oder die Leiden lindert? Oder handeln, Ärzte und Angehörige unethisch, wenn sie aus ethischen Gründen die Leiden eines Patienten in Kauf nehmen?
(Zeichnung: Sheree Domingo, 2019)
Ein weiteres Denkmodell wäre es, mit anderen Länder und Kulturen in den Diskurs zu treten und sie letztlich von unseren ethischen Auffassungen zu überzeugen. Ob eine solche „Missionierung“ angemessen ist, möchte ich bezweifeln. Sie impliziert eine Überlegenheit unserer Ethik gegenüber anderen Kulturen und kann im Extremfall so interpretiert werden, dass wir ihnen ethische Kompetenzen absprechen.
Wenn wir einerseits unsere wissenschaftliche Kompetenz und Expertise und andererseits unsere ethischen Ansprüche erhalten wollen (zu beidem sind wir m.E. ethisch verpflichtet), müssen wir doppelte Anstrengungen leisten und, trotz aller selbst auferlegten Hürden, Exzellenz und Innovation liefern. Ein wortgewaltiger „Lehrmeister“, der gleichzeitig zeigt, dass mit seinen ethischen Maximen keine Innovationen zum Wohle der Menschheit erzielt werden, wird keine Vorbildfunktion einnehmen können.
Das wird zunehmend schwieriger. Sowohl bei der wissenschaftlichen Kompetenz als auch beim technologischen Know-How haben andere Länder, vor allem China, gewaltig aufgeholt und befinden sich mindestens auf Augenhöhe mit den früher führenden Wissenschaftsnationen. Wir müssen diese Herausforderung annehmen.
Danksagung:
Ich danke Jann Buttlar für kritische Kommentare zum Manuskript
Disclaimer:
Dieser Artikel stellt die persönliche Sicht des Autors dar. Er stellt keinen Anspruch auf die „einzig richtige Betrachtungsweise“ sondern soll zur Diskussion anregen.
Autor:
Wolfgang Nellen, BioWissKomm

